關(guān)于申報(bào)2022年度生物醫(yī)藥企業(yè)研發(fā)創(chuàng)新補(bǔ)助、產(chǎn)業(yè)化獎(jiǎng)勵(lì)及新業(yè)態(tài)投資配套獎(jiǎng)勵(lì)的通知
2022年度生物醫(yī)藥企業(yè)研發(fā)創(chuàng)新補(bǔ)助、產(chǎn)業(yè)化獎(jiǎng)勵(lì)、新業(yè)態(tài)投資配套獎(jiǎng)勵(lì)開始申報(bào),現(xiàn)通知如下:
一、本次兌現(xiàn)范圍:
1、本次兌現(xiàn)適用于在海滄區(qū)進(jìn)行商事登記和稅務(wù)登記,具有獨(dú)立法人資格,并從事包括藥品、醫(yī)療器械、醫(yī)用衛(wèi)生材料、保化品、特殊醫(yī)學(xué)用途配方食品等領(lǐng)域的研發(fā)、生產(chǎn)、流通、技術(shù)服務(wù)的企業(yè)和機(jī)構(gòu),以及為產(chǎn)業(yè)配套的核心零部件及關(guān)鍵原材料研發(fā)、生產(chǎn)的企業(yè)。
2、研發(fā)創(chuàng)新平臺(tái)補(bǔ)助:對(duì)2022年度新認(rèn)定的重點(diǎn)實(shí)驗(yàn)室、工程研究中心、技術(shù)創(chuàng)新中心、產(chǎn)業(yè)創(chuàng)新中心、制造業(yè)創(chuàng)新中心、企業(yè)技術(shù)中心、博士后科研工作站,按照國家級(jí)、省(市)級(jí)不同等次給予最高300萬、100萬元獎(jiǎng)勵(lì)。單個(gè)企業(yè)按就高不重復(fù)原則享受本項(xiàng)獎(jiǎng)勵(lì)。
3、新藥研發(fā)補(bǔ)助:(1)對(duì)創(chuàng)新藥(1類化學(xué)藥品、1類生物制品、中藥創(chuàng)新藥,下同),完成臨床前研究并獲得臨床批件或默許臨床的,給予100萬元補(bǔ)助;完成I期臨床試驗(yàn)并進(jìn)入Ⅱ期臨床試驗(yàn)的,給予100萬元補(bǔ)助;完成Ⅱ期臨床試驗(yàn)并進(jìn)入Ⅲ期臨床試驗(yàn)的,給予200萬元補(bǔ)助;完成Ⅲ期臨床試驗(yàn)并取得注冊(cè)批件的,給予400萬元補(bǔ)助。(2)對(duì)改良型新藥(2類化學(xué)藥品、2類生物制品、中藥改良型新藥,下同),完成臨床前研究并獲得臨床批件或默許臨床的,給予100萬元補(bǔ)助;完成I期臨床試驗(yàn)并進(jìn)入Ⅱ期臨床試驗(yàn)的,給予100萬元補(bǔ)助;完成Ⅱ期臨床試驗(yàn)并進(jìn)入Ⅲ期臨床試驗(yàn)的,給予150萬元補(bǔ)助;完成Ⅲ期臨床試驗(yàn)并取得注冊(cè)批件的,給予300萬元補(bǔ)助。(3)仿制藥研發(fā)補(bǔ)助:對(duì)通過(含視同通過)質(zhì)量和療效一致性評(píng)價(jià)或臨床有效性試驗(yàn)取得藥品注冊(cè)批件或藥品補(bǔ)充申請(qǐng)批件的仿制藥品種,每個(gè)品種給予100萬元補(bǔ)助。
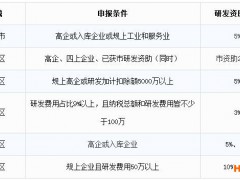
3、產(chǎn)業(yè)化獎(jiǎng)勵(lì):(1)對(duì)取得創(chuàng)新藥、改良型新藥、仿制藥(含3類化學(xué)藥品、4類化學(xué)藥品、3類生物制品、古代經(jīng)典名方中藥復(fù)方制劑、中藥同名同方藥)藥品注冊(cè)證書且該產(chǎn)品首次在海滄區(qū)實(shí)業(yè)產(chǎn)業(yè)化(取證后累計(jì)銷售收入達(dá)100萬以上)的,按照每種產(chǎn)品分別給予300萬、150萬、100萬元獎(jiǎng)勵(lì)。(2)對(duì)第二、第三類醫(yī)療器械取得注冊(cè)證書且該產(chǎn)品首次在海滄區(qū)實(shí)業(yè)產(chǎn)業(yè)化(取證后累計(jì)銷售達(dá)20萬以上)的,按照類別每種產(chǎn)品分別給予20萬、80萬元獎(jiǎng)勵(lì)。單個(gè)企業(yè)每年補(bǔ)助金額最高不超過500萬元。
4、新業(yè)態(tài)投資配套獎(jiǎng)勵(lì):對(duì)生物醫(yī)藥合同研發(fā)機(jī)構(gòu)(CRO)、合同外包機(jī)構(gòu)(CMO)、合同定制研發(fā)生產(chǎn)機(jī)構(gòu)(CDMO)等產(chǎn)業(yè)應(yīng)用基礎(chǔ)平臺(tái)建設(shè)項(xiàng)目,按照獲得市級(jí)相應(yīng)固定資產(chǎn)投入補(bǔ)助的50%予以配套補(bǔ)助,最高不超過200萬元。
二、需提交的資料清單
1、兌現(xiàn)研發(fā)創(chuàng)新平臺(tái)補(bǔ)助的,提交以下資料:
(1)《海滄區(qū)生物與新醫(yī)藥企業(yè)補(bǔ)助申請(qǐng)表》。
(2) 2022年度新認(rèn)定的平臺(tái)文件或證書。
2、兌現(xiàn)新藥研發(fā)補(bǔ)助的,提交以下資料:
(1)《海滄區(qū)生物與新醫(yī)藥企業(yè)補(bǔ)助申請(qǐng)表》。
(2) 新藥臨床試驗(yàn)各階段的臨床試驗(yàn)合同、獲得的注冊(cè)批件等階段性材料。
3、兌現(xiàn)創(chuàng)新藥、改良型新藥、仿制藥產(chǎn)業(yè)化獎(jiǎng)勵(lì)的,提交以下資料:
(1)《海滄區(qū)生物與新醫(yī)藥企業(yè)補(bǔ)助申請(qǐng)表》。
(2)2022年度財(cái)務(wù)審計(jì)報(bào)告。
(3)申報(bào)產(chǎn)品品種銷售收入專項(xiàng)審計(jì)報(bào)告。
4、兌現(xiàn)醫(yī)療器械產(chǎn)業(yè)化獎(jiǎng)勵(lì)的,提交以下資料:
(1)《海滄區(qū)生物與新醫(yī)藥企業(yè)補(bǔ)助申請(qǐng)表》
(2)醫(yī)療器械產(chǎn)品注冊(cè)證書(二類還需提交產(chǎn)品登記表、三類還需提交受理通知書)。
(3)申報(bào)產(chǎn)品品種銷售收入專項(xiàng)審計(jì)報(bào)告。
5、兌現(xiàn)新業(yè)態(tài)投資配套獎(jiǎng)勵(lì),提交以下資料:
(1)《海滄區(qū)生物與新醫(yī)藥企業(yè)補(bǔ)助申請(qǐng)表》。
(2)平臺(tái)資質(zhì)文件。
(3)獲得市級(jí)相應(yīng)固定資產(chǎn)投入補(bǔ)助的證明材料。
上述資料一式二份,除申請(qǐng)表需要原件外,其余材料需復(fù)印件蓋單。
三、申報(bào)受理
1、受理時(shí)間:2023年3月30日至2023年4月15日
2、受理方式:將材料遞交至生物醫(yī)藥產(chǎn)業(yè)園B1棟11樓(廈門海滄翁角西路2050號(hào)11樓1112室)
四、其他事項(xiàng)
申報(bào)企業(yè)若以虛假材料惡意套取補(bǔ)助經(jīng)費(fèi),區(qū)工信局將收回全額資助資金、記入企業(yè)誠信檔案,若涉嫌違法犯罪的,將依法移交相關(guān)部門處理。
附件:《海滄區(qū)生物與新醫(yī)藥企業(yè)補(bǔ)助申請(qǐng)表》
廈門市海滄區(qū)工信局
廈門海滄生物科技發(fā)展有限公司
2023年3月29日
中企檢測認(rèn)證網(wǎng)提供iso體系認(rèn)證機(jī)構(gòu)查詢,檢驗(yàn)檢測、認(rèn)證認(rèn)可、資質(zhì)資格、計(jì)量校準(zhǔn)、知識(shí)產(chǎn)權(quán)貫標(biāo)一站式行業(yè)企業(yè)服務(wù)平臺(tái)。中企檢測認(rèn)證網(wǎng)為檢測行業(yè)相關(guān)檢驗(yàn)、檢測、認(rèn)證、計(jì)量、校準(zhǔn)機(jī)構(gòu),儀器設(shè)備、耗材、配件、試劑、標(biāo)準(zhǔn)品供應(yīng)商,法規(guī)咨詢、標(biāo)準(zhǔn)服務(wù)、實(shí)驗(yàn)室軟件提供商提供包括品牌宣傳、產(chǎn)品展示、技術(shù)交流、新品推薦等全方位推廣服務(wù)。這個(gè)問題就給大家解答到這里了,如還需要了解更多專業(yè)性問題可以撥打中企檢測認(rèn)證網(wǎng)在線客服13550333441。為您提供全面檢測、認(rèn)證、商標(biāo)、專利、知識(shí)產(chǎn)權(quán)、版權(quán)法律法規(guī)知識(shí)資訊,包括商標(biāo)注冊(cè)、食品檢測、第三方檢測機(jī)構(gòu)、網(wǎng)絡(luò)信息技術(shù)檢測、環(huán)境檢測、管理體系認(rèn)證、服務(wù)體系認(rèn)證、產(chǎn)品認(rèn)證、版權(quán)登記、專利申請(qǐng)、知識(shí)產(chǎn)權(quán)、檢測法、認(rèn)證標(biāo)準(zhǔn)等信息,中企檢測認(rèn)證網(wǎng)為檢測認(rèn)證商標(biāo)專利從業(yè)者提供多種檢測、認(rèn)證、知識(shí)產(chǎn)權(quán)、版權(quán)、商標(biāo)、專利的轉(zhuǎn)讓代理查詢法律法規(guī),咨詢輔導(dǎo)等知識(shí)。
本文內(nèi)容整合網(wǎng)站:中國政府網(wǎng)、百度百科、最高人民法院、知乎、國家認(rèn)證認(rèn)可監(jiān)督管理委員會(huì)、國家知識(shí)產(chǎn)權(quán)局、市場監(jiān)督總局
免責(zé)聲明:本文部分內(nèi)容根據(jù)網(wǎng)絡(luò)信息整理,文章版權(quán)歸原作者所有。向原作者致敬!發(fā)布旨在積善利他,如涉及作品內(nèi)容、版權(quán)和其它問題,請(qǐng)跟我們聯(lián)系刪除并致歉!