醫(yī)療器械FDA認(rèn)證I,II或III類(lèi)設(shè)備怎么區(qū)分?
美國(guó)FDA規(guī)范在美國(guó)銷(xiāo)售的所有醫(yī)療器械,這些醫(yī)療器械分為三大類(lèi)。FDA批準(zhǔn)的任何醫(yī)療器械都將根據(jù)其風(fēng)險(xiǎn),侵襲性以及對(duì)患者總體健康的影響分為I,II或III類(lèi)。
但是,這三個(gè)類(lèi)別之間的界限在哪里,為什么?
美國(guó)FDA的分類(lèi)準(zhǔn)則可能會(huì)使醫(yī)療器械制造商對(duì)系統(tǒng)的接觸程度極度混亂。根據(jù)設(shè)備的分組方式,制造商的最佳市場(chǎng)開(kāi)發(fā)途徑存在巨大差異。與II類(lèi)或III類(lèi)設(shè)備相比,I類(lèi)設(shè)備受到的法規(guī)要求要少得多。
通過(guò)了解FDA醫(yī)療器械類(lèi)別中的差異,您可以了解如何對(duì)器械進(jìn)行分組。掌握了這些知識(shí)后,處于上市前階段的醫(yī)療設(shè)備制造商可以更好地準(zhǔn)備和分配監(jiān)管批準(zhǔn)所需的資源。

FDA醫(yī)療器械類(lèi)別之間的差異:
FDA已經(jīng)對(duì)1,700多種不同類(lèi)型的醫(yī)療設(shè)備進(jìn)行了分類(lèi)。這些設(shè)備按照16種專(zhuān)業(yè)分類(lèi)在《聯(lián)邦法規(guī)(CFR)》中,例如心血管或血液學(xué)設(shè)備。根據(jù)16種專(zhuān)業(yè)中的一種對(duì)醫(yī)療設(shè)備進(jìn)行分類(lèi)是了解您是否要制造I,II或III級(jí)醫(yī)療設(shè)備的第一步。
根據(jù)專(zhuān)業(yè)對(duì)設(shè)備進(jìn)行分類(lèi)后,F(xiàn)DA指示制造商在了解其設(shè)備是否獲豁免的情況下進(jìn)行上市前通知。風(fēng)險(xiǎn)和侵入性最低的I類(lèi)醫(yī)療設(shè)備免于上市前通知流程。特定的II類(lèi)設(shè)備也無(wú)需獲得上市前批準(zhǔn)。
但是,由FDA監(jiān)管的所有設(shè)備都必須遵守有關(guān)注冊(cè),標(biāo)簽和質(zhì)量的當(dāng)前良好生產(chǎn)規(guī)范(cGMP)要求。但是,您如何知道您的設(shè)備是I類(lèi)還是II類(lèi),以及是否需要接受售前通知?
醫(yī)療FDA認(rèn)證3大分類(lèi):
1.醫(yī)療器械FDA注冊(cè)1類(lèi)設(shè)備:
美國(guó)食品和藥物管理局將I類(lèi)設(shè)備定義為“ 不旨在用于維持生命或維持生命,或在防止危害人類(lèi)健康方面具有重要意義,并且可能不存在潛在的不合理疾病或傷害風(fēng)險(xiǎn)的設(shè)備 ”。
這些設(shè)備是FDA監(jiān)管的最常見(jiàn)的設(shè)備類(lèi)別,占市場(chǎng)上批準(zhǔn)的設(shè)備的47%。
I類(lèi)設(shè)備與患者的接觸最少,對(duì)患者的整體健康影響很小。通常,I類(lèi)設(shè)備不會(huì)與患者的內(nèi)部器官,中樞神經(jīng)系統(tǒng)或心血管系統(tǒng)接觸。這些設(shè)備受最少的法規(guī)要求。
I類(lèi)設(shè)備的示例:
1.電動(dòng)牙刷
2.壓舌板
3.氧氣面罩
4.可重復(fù)使用的手術(shù)刀
5.繃帶
6.醫(yī)院病床
將I類(lèi)醫(yī)療設(shè)備推向美國(guó)市場(chǎng):
I類(lèi)設(shè)備是最快,最容易推向市場(chǎng)的設(shè)備,因?yàn)樗鼈兘o患者帶來(lái)的風(fēng)險(xiǎn)最小,并且對(duì)維持生命的護(hù)理至關(guān)重要。大部分I類(lèi)設(shè)備免于FDA的上市前通知(510k)和上市前批準(zhǔn)(PMA)要求。
I類(lèi)設(shè)備不受FDA通用控制的豁免,F(xiàn)DA通用控制是一系列適用于I,II和III類(lèi)醫(yī)療設(shè)備的命令。該法案的規(guī)定涉及摻假,商標(biāo)錯(cuò)誤,設(shè)備注冊(cè),記錄和良好生產(chǎn)規(guī)范。仍屬于A類(lèi)的醫(yī)療器械制造商仍必須實(shí)施質(zhì)量管理體系并遵循標(biāo)準(zhǔn)以確保產(chǎn)品質(zhì)量。
相關(guān)閱讀:上市前通知510(k)與上市前批準(zhǔn)之間的區(qū)別
2.醫(yī)療器械FDA注冊(cè)II類(lèi)設(shè)備:
II類(lèi)醫(yī)療設(shè)備比I類(lèi)醫(yī)療設(shè)備更為復(fù)雜,并且存在較高的風(fēng)險(xiǎn)類(lèi)別,因?yàn)樗鼈兏赡芘c患者持續(xù)接觸。這可能包括與患者的心血管系統(tǒng)或內(nèi)部器官接觸的設(shè)備以及診斷工具。
FDA將II類(lèi)設(shè)備定義為“ 其通用控制措施不足以合理保證設(shè)備安全性和有效性的設(shè)備”。”
II類(lèi)醫(yī)療設(shè)備的示例:
1.導(dǎo)尿管
2.血壓袖套
3.懷孕測(cè)試包
4.針筒
5.輸血套件
6.隱形眼鏡
7.手術(shù)手套
8.可吸收縫線
將II類(lèi)醫(yī)療設(shè)備推向美國(guó)市場(chǎng)
控件因設(shè)備而異,但根據(jù)FDA的規(guī)定,可以包括:
1.設(shè)備性能
2.上市后監(jiān)控
3.病人登記
4.特殊標(biāo)簽要求
5.上市前數(shù)據(jù)要求
指導(dǎo)方針
大多數(shù)II類(lèi)設(shè)備已通過(guò)“上市前通知”或510(k)程序獲得FDA批準(zhǔn)投放市場(chǎng)。
II類(lèi)設(shè)備受到上述相同的通用控制的約束,但FDA將其定義為“對(duì)其通用控制不足以提供合理保證該設(shè)備安全性和有效性的設(shè)備”。因此,II類(lèi)設(shè)備也要接受特殊控制。這些法規(guī)取決于設(shè)備,并且可能包括特殊的標(biāo)簽要求,患者注冊(cè)表和性能標(biāo)準(zhǔn)。
大多數(shù)II類(lèi)設(shè)備通過(guò)售前通知(510k)流程進(jìn)入市場(chǎng)。510(k)是FDA的復(fù)雜應(yīng)用程序,它通過(guò)證明該設(shè)備與市場(chǎng)上的其他設(shè)備等效來(lái)證明該設(shè)備是安全有效的。
此過(guò)程涉及顯示與另一種設(shè)備的“實(shí)質(zhì)等效性”,這在FDA術(shù)語(yǔ)中稱(chēng)為“謂詞”。這并不意味著設(shè)備需要相同,但是它們?cè)谑褂茫O(shè)計(jì),材料,標(biāo)簽,標(biāo)準(zhǔn)和其他特性上需要相當(dāng)?shù)南嗨菩浴?/p>
FDA在2018年初發(fā)布了一份豁免清單,該清單免除了510(k)程序中的800多種通用I類(lèi)和II類(lèi)醫(yī)療設(shè)備。如果您擁有通用的II類(lèi)醫(yī)療設(shè)備,則可以通過(guò)搜索FDA產(chǎn)品分類(lèi)數(shù)據(jù)庫(kù)來(lái)發(fā)現(xiàn)其是否免于510(k)備案。
相關(guān)閱讀:徹底改革FDA 510(k)的5個(gè)理由是一個(gè)重大舉措。
3、醫(yī)療器械FDA將III類(lèi)設(shè)備:
FDA將III類(lèi)設(shè)備定義為“通常會(huì)維持或維持生命,被植入或存在潛在的不合理疾病或受傷風(fēng)險(xiǎn)”的產(chǎn)品。
美國(guó)FDA監(jiān)管的設(shè)備中只有10%屬于III類(lèi)。此分類(lèi)通常擴(kuò)展到永久性植入物,智能醫(yī)療設(shè)備和生命支持系統(tǒng)。
雖然通常將III類(lèi)保留給最具創(chuàng)新性和最先進(jìn)的醫(yī)療設(shè)備,但由于其他原因,還有其他一些設(shè)備可以歸入III類(lèi)。如果制造商在PMA(510k)歸檔過(guò)程中無(wú)法證明與謂詞(現(xiàn)有產(chǎn)品)的實(shí)質(zhì)等同性,則某些最初歸類(lèi)為II類(lèi)的設(shè)備可能會(huì)升為III類(lèi)。
III類(lèi)醫(yī)療設(shè)備的示例:
1.乳房植入物
2.起搏器
3.除顫器
4.高頻呼吸機(jī)
5.人工耳蝸
6.胎兒血液采樣儀
7.植入假肢
將III類(lèi)醫(yī)療設(shè)備推向美國(guó)市場(chǎng):
III類(lèi)設(shè)備受所有FDA通用控制和FDA上市前批準(zhǔn)(PMA)流程的約束。FDA寫(xiě)道:“由于與III類(lèi)設(shè)備相關(guān)的風(fēng)險(xiǎn)水平,F(xiàn)DA已經(jīng)確定僅常規(guī)和特殊控制不足以確保III類(lèi)設(shè)備的安全性和有效性。”
PMA是FDA要求的最密集的設(shè)備營(yíng)銷(xiāo)應(yīng)用程序。某些FDA III類(lèi)設(shè)備是免稅的,并且可能符合510(k)備案的要求,但是大多數(shù)都有望獲得上市前批準(zhǔn)。
PMA流程需要對(duì)醫(yī)療器械進(jìn)行嚴(yán)格的研究,以通過(guò)開(kāi)發(fā)數(shù)據(jù)驅(qū)動(dòng)的利益/風(fēng)險(xiǎn)檔案來(lái)證明安全性和有效性。PMA過(guò)程通常涉及臨床試驗(yàn)以及大量時(shí)間和資源,以進(jìn)行足夠的數(shù)據(jù)收集。III類(lèi)中PMA流程的唯一例外是具有相當(dāng)?shù)刃Чδ艿脑O(shè)備。您可以通過(guò)搜索FDA 上市前批準(zhǔn)(PMA)數(shù)據(jù)庫(kù)和510(k)上市前通知數(shù)據(jù)庫(kù)確定是否可以使用510(k)來(lái)銷(xiāo)售III類(lèi)設(shè)備。
怎么確定FDA注冊(cè)類(lèi)別?
對(duì)您的醫(yī)療設(shè)備進(jìn)行分類(lèi)的第一步是瀏覽FDA分類(lèi)法規(guī),即根據(jù)醫(yī)療專(zhuān)業(yè)劃分的16種醫(yī)療設(shè)備類(lèi)別列表。
例如,我們將向您展示識(shí)別血壓報(bào)警器分類(lèi)的步驟。該設(shè)備被歸類(lèi)為870類(lèi):心血管設(shè)備。

找到相關(guān)的醫(yī)學(xué)專(zhuān)業(yè)后,單擊類(lèi)別,然后瀏覽設(shè)備列表,直到找到等效的內(nèi)容和關(guān)聯(lián)的設(shè)備代碼。

單擊設(shè)備代碼并打開(kāi)準(zhǔn)則。設(shè)備分類(lèi)在(b)節(jié)中列出。
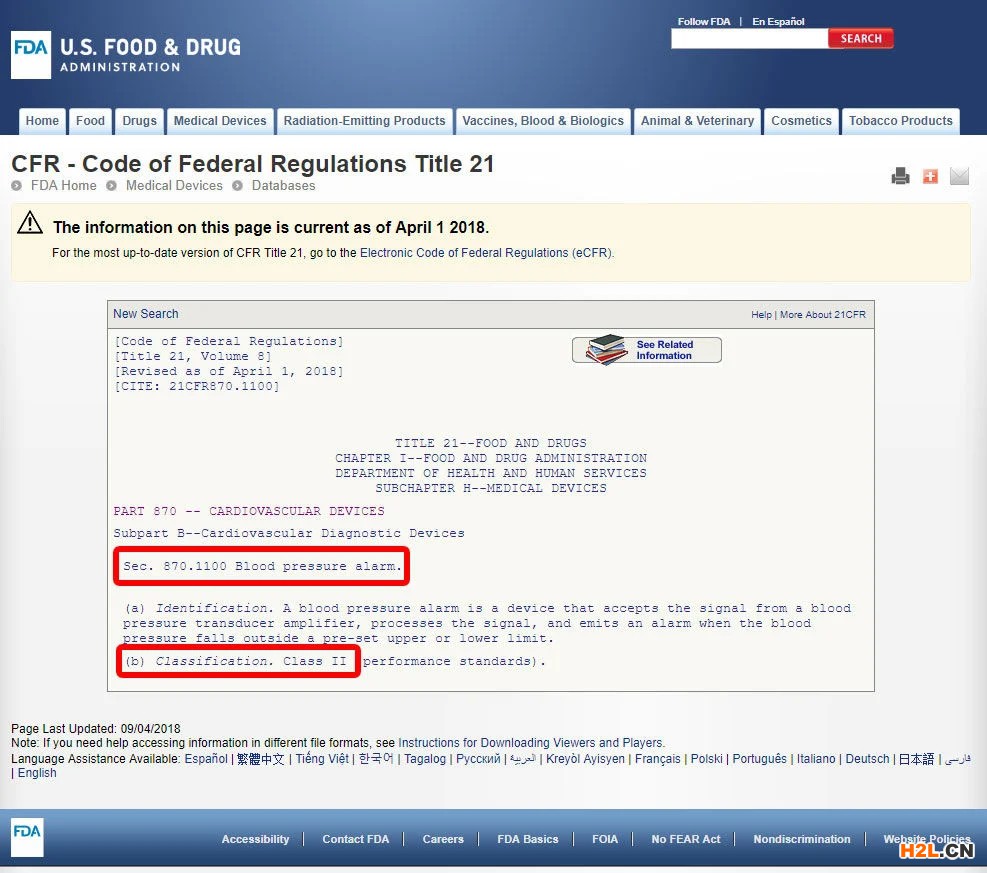
如果您的設(shè)備在FDA分類(lèi)的1700種設(shè)備中缺少列出的同等產(chǎn)品,則很可能是沒(méi)有實(shí)質(zhì)性等效產(chǎn)品的創(chuàng)新設(shè)備,將被歸類(lèi)為III類(lèi)。
了解FDA醫(yī)療器械類(lèi)別
被FDA分類(lèi)為I,II或III級(jí)的醫(yī)療設(shè)備之間的差異主要在于風(fēng)險(xiǎn),與患者及其內(nèi)部系統(tǒng)的接觸量以及設(shè)備是否對(duì)維持生命至關(guān)重要。
除了這些因素之外,F(xiàn)DA在確定設(shè)備的分類(lèi)方式時(shí)還考慮了相當(dāng)?shù)牡刃浴H绻脑O(shè)備風(fēng)險(xiǎn)低并且與患者的接觸最少,則您很可能有資格獲得I類(lèi)和簡(jiǎn)化的市場(chǎng)批準(zhǔn)程序。II類(lèi)和III類(lèi)設(shè)備必須通過(guò)實(shí)質(zhì)等效性,510(k)備案或上市前批準(zhǔn)流程證明其安全性。
通過(guò)了解您的設(shè)備如何分類(lèi),您可以通過(guò)了解FDA可能需要的過(guò)程和文件來(lái)簡(jiǎn)化獲得市場(chǎng)認(rèn)可的途徑。如果您的組織受到II級(jí)或III級(jí)510(k)或PMA的要求,則此知識(shí)可以幫助您提前分配適當(dāng)?shù)馁Y源并計(jì)劃成功的申請(qǐng)。
中企檢測(cè)認(rèn)證網(wǎng)提供iso體系認(rèn)證機(jī)構(gòu)查詢,檢驗(yàn)檢測(cè)、認(rèn)證認(rèn)可、資質(zhì)資格、計(jì)量校準(zhǔn)、知識(shí)產(chǎn)權(quán)貫標(biāo)一站式行業(yè)企業(yè)服務(wù)平臺(tái)。中企檢測(cè)認(rèn)證網(wǎng)為檢測(cè)行業(yè)相關(guān)檢驗(yàn)、檢測(cè)、認(rèn)證、計(jì)量、校準(zhǔn)機(jī)構(gòu),儀器設(shè)備、耗材、配件、試劑、標(biāo)準(zhǔn)品供應(yīng)商,法規(guī)咨詢、標(biāo)準(zhǔn)服務(wù)、實(shí)驗(yàn)室軟件提供商提供包括品牌宣傳、產(chǎn)品展示、技術(shù)交流、新品推薦等全方位推廣服務(wù)。這個(gè)問(wèn)題就給大家解答到這里了,如還需要了解更多專(zhuān)業(yè)性問(wèn)題可以撥打中企檢測(cè)認(rèn)證網(wǎng)在線客服13550333441。為您提供全面檢測(cè)、認(rèn)證、商標(biāo)、專(zhuān)利、知識(shí)產(chǎn)權(quán)、版權(quán)法律法規(guī)知識(shí)資訊,包括商標(biāo)注冊(cè)、食品檢測(cè)、第三方檢測(cè)機(jī)構(gòu)、網(wǎng)絡(luò)信息技術(shù)檢測(cè)、環(huán)境檢測(cè)、管理體系認(rèn)證、服務(wù)體系認(rèn)證、產(chǎn)品認(rèn)證、版權(quán)登記、專(zhuān)利申請(qǐng)、知識(shí)產(chǎn)權(quán)、檢測(cè)法、認(rèn)證標(biāo)準(zhǔn)等信息,中企檢測(cè)認(rèn)證網(wǎng)為檢測(cè)認(rèn)證商標(biāo)專(zhuān)利從業(yè)者提供多種檢測(cè)、認(rèn)證、知識(shí)產(chǎn)權(quán)、版權(quán)、商標(biāo)、專(zhuān)利的轉(zhuǎn)讓代理查詢法律法規(guī),咨詢輔導(dǎo)等知識(shí)。
本文內(nèi)容整合網(wǎng)站:百度百科、搜狗百科、360百科、知乎、市場(chǎng)監(jiān)督總局 、國(guó)家認(rèn)證認(rèn)可監(jiān)督管理委員會(huì)、質(zhì)量認(rèn)證中心
免責(zé)聲明:本文部分內(nèi)容根據(jù)網(wǎng)絡(luò)信息整理,文章版權(quán)歸原作者所有。向原作者致敬!發(fā)布旨在積善利他,如涉及作品內(nèi)容、版權(quán)和其它問(wèn)題,請(qǐng)跟我們聯(lián)系刪除并致歉!
本文來(lái)源: http://m.rumin8raps.com/zs/202011/ccaa_11143.html